開篇宣告:1:以下內容轉自以下內容轉自微信公眾號滬上臨研人《著名Global臨床CRO在我國因監查問題被FDA認定為“VAI”》,如有侵權,可聯絡刪除
2. 以下觀點,僅代表作者個人觀點,請帶著質疑的態度去閱讀。如有問題,歡迎評論區留言或直接聯絡作者
近日,美國食品藥品監督管理局(FDA)公佈的四月份對中國臨床試驗現場的核查結果中,一家知名全球臨床CRO因監查問題被判定為“VAI”(自願採取行政措施)。這一結果在業內引發廣泛關注。

我們再來回顧下美國臨床試驗現場覈查的結論。
根據FDA官方指南,現場檢查結果分為三級:
NAI:“不需要採取行政措施”
VAI:“發現問題,自願採取行政措施”
OAI:“嚴重問題,需要採取官方行政措施”
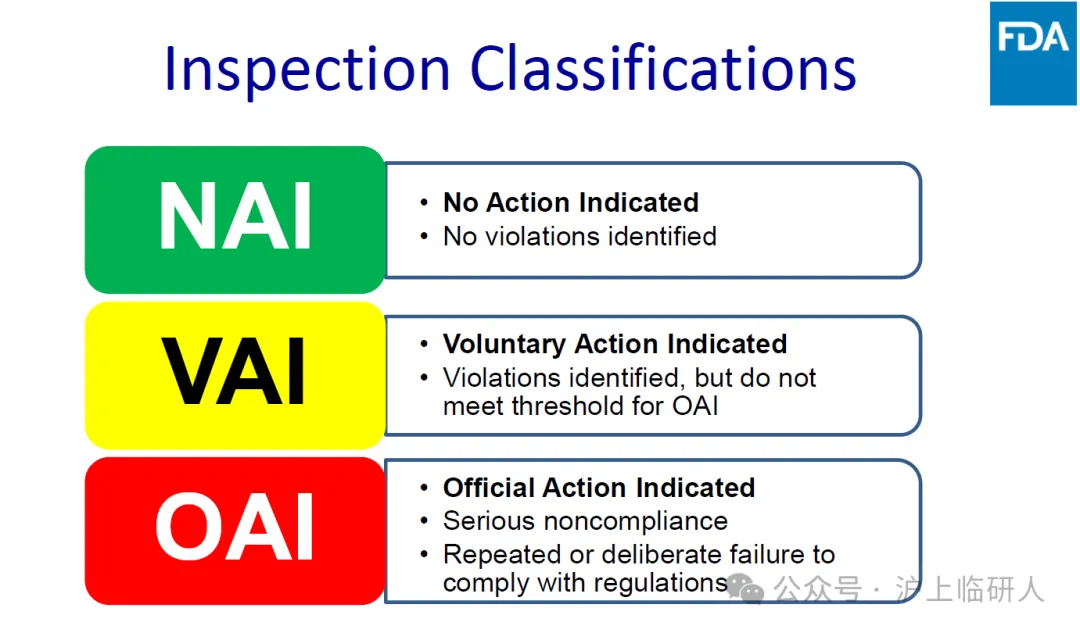
簡單來說,NAI是"優秀生",VAI是"有進步空間",OAI則是"亮紅燈"。
值得注意的是,VAI雖非最嚴重級別,但對一家服務全球藥企的CRO而言,絕非"小事一樁"。要知道,這類機構往往同時參與多個跨國試驗,監查體系的漏洞可能影響的不只是一兩個專案,更是整個中國臨床研究在國際上的信譽背書。
"VAI"背後:是個案,還是行業共性問題?
事件發酵後,業內有兩種聲音:
有人說,這不過是"個別員工操作失誤";也有人追問:"全球CRO的質控體系,難道沒兜住?"
事實上,這恰恰戳中了當前中國臨床研究的"成長痛點"——能力上去了,合規意識和管理細節還在追趕。
從行業資料看,FDA對臨床試驗的檢查中,監查缺陷長期位列常見問題前三。比如:
監查計劃流於形式,未針對試驗風險設計個性化策略;
對研究中心的原始資料覈查(SDV)覆蓋不全,關鍵資料偏差未被及時發現;
與研究者溝通僅停留在"進度跟進",未深入排查潛在GCP風險。
更關鍵的是,這類問題往往不是"單點失誤",而是管理體系的隱性漏洞。舉個例子:如果CRO的監查員培訓只側重"查什麼",卻沒教"怎麼判斷風險優先順序";如果質量部門只抽查報告,不追溯原始記錄的核查邏輯——再資深的團隊也可能在細節上栽跟頭。
中國臨床研究的"雙面映象":進步與挑戰並存
當然,我們也不能因一次"VAI"否定整個行業的努力。事實上,中國臨床研究機構的合規能力正在肉眼可見地提升。中國臨床研究不僅能"做試驗",更能"做好合規的試驗"。但此次全球CRO的VAI事件也提醒我們:合規不是"達標即止",而是需要持續迭代的"動態能力"。
給行業的一點建議:把合規刻進"肌肉記憶"
面對越來越頻繁的國際覈查,無論是CRO還是本土臨床試驗機構,或許該從這三件事做起:
1. 把"風險思維"嵌入監查全流程
監查不是"按清單打鉤",而是基於試驗階段、適應症特點、研究中心歷史資料的風險分級。比如腫瘤藥試驗的患者脫落率、慢性病試驗的隨訪依從性,都需要定製化監查策略。
2. 讓"質量文化"穿透每個環節
從CRA的入職培訓,到管理層的季度質量覆盤,都要把"合規不是負擔,是競爭力"的理念傳遞到位。某頭部CRO的做法值得參考:他們每月公佈各專案的"質量健康度評分",直接與團隊績效掛鉤。
3. 用"模擬檢查"練出"臨場免疫力"
與其等FDA來查,不如自己當"考官"。定期組織內部模擬覈查,甚至邀請國際QMS專家挑刺,把潛在問題消滅在"預演"階段。
反思
FDA的VAI結論,與其說是"批評",不如說是給中國臨床研究的"成長提示"。
當中國創新藥開始在全球舞臺嶄露頭角,我們的臨床試驗能力也必須完成從"跟跑"到"並跑"的跨越。這不僅需要技術突破,更需要用國際最高標準打磨每一個操作細節。
畢竟,在FDA的眼裏,沒有"差不多",只有"合規即底線"。
願下一次,中國CRO交出的核查答卷,寫滿"NAI"。
完結













0則評論