开篇声明:1:以下内容转自以下内容转自微信公众号沪上临研人《著名Global临床CRO在我国因监查问题被FDA认定为“VAI”》,如有侵权,可联系删除
2. 以下观点,仅代表作者个人观点,请带着质疑的态度去阅读。如有问题,欢迎评论区留言或直接联系作者
近日,美国食品药品监督管理局(FDA)公布的四月份对中国临床试验现场的核查结果中,一家知名全球临床CRO因监查问题被判定为“VAI”(自愿采取行政措施)。这一结果在业内引发广泛关注。

我们再来回顾下美国临床试验现场核查的结论。
根据FDA官方指南,现场检查结果分为三级:
NAI:“不需要采取行政措施”
VAI:“发现问题,自愿采取行政措施”
OAI:“严重问题,需要采取官方行政措施”
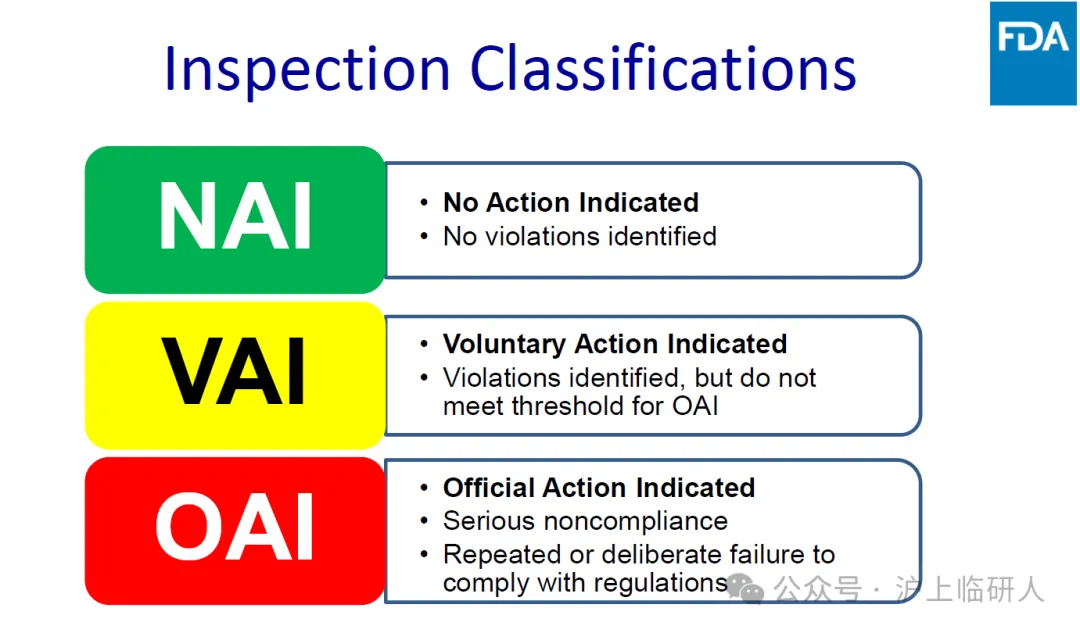
简单来说,NAI是"优秀生",VAI是"有进步空间",OAI则是"亮红灯"。
值得注意的是,VAI虽非最严重级别,但对一家服务全球药企的CRO而言,绝非"小事一桩"。要知道,这类机构往往同时参与多个跨国试验,监查体系的漏洞可能影响的不只是一两个项目,更是整个中国临床研究在国际上的信誉背书。
"VAI"背后:是个案,还是行业共性问题?
事件发酵后,业内有两种声音:
有人说,这不过是"个别员工操作失误";也有人追问:"全球CRO的质控体系,难道没兜住?"
事实上,这恰恰戳中了当前中国临床研究的"成长痛点"——能力上去了,合规意识和管理细节还在追赶。
从行业数据看,FDA对临床试验的检查中,监查缺陷长期位列常见问题前三。比如:
监查计划流于形式,未针对试验风险设计个性化策略;
对研究中心的原始数据核查(SDV)覆盖不全,关键数据偏差未被及时发现;
与研究者沟通仅停留在"进度跟进",未深入排查潜在GCP风险。
更关键的是,这类问题往往不是"单点失误",而是管理体系的隐性漏洞。举个例子:如果CRO的监查员培训只侧重"查什么",却没教"怎么判断风险优先级";如果质量部门只抽查报告,不追溯原始记录的核查逻辑——再资深的团队也可能在细节上栽跟头。
中国临床研究的"双面镜像":进步与挑战并存
当然,我们也不能因一次"VAI"否定整个行业的努力。事实上,中国临床研究机构的合规能力正在肉眼可见地提升。中国临床研究不仅能"做试验",更能"做好合规的试验"。但此次全球CRO的VAI事件也提醒我们:合规不是"达标即止",而是需要持续迭代的"动态能力"。
给行业的一点建议:把合规刻进"肌肉记忆"
面对越来越频繁的国际核查,无论是CRO还是本土临床试验机构,或许该从这三件事做起:
1. 把"风险思维"嵌入监查全流程
监查不是"按清单打钩",而是基于试验阶段、适应症特点、研究中心历史数据的风险分级。比如肿瘤药试验的患者脱落率、慢性病试验的随访依从性,都需要定制化监查策略。
2. 让"质量文化"穿透每个环节
从CRA的入职培训,到管理层的季度质量复盘,都要把"合规不是负担,是竞争力"的理念传递到位。某头部CRO的做法值得参考:他们每月公布各项目的"质量健康度评分",直接与团队绩效挂钩。
3. 用"模拟检查"练出"临场免疫力"
与其等FDA来查,不如自己当"考官"。定期组织内部模拟核查,甚至邀请国际QMS专家挑刺,把潜在问题消灭在"预演"阶段。
反思
FDA的VAI结论,与其说是"批评",不如说是给中国临床研究的"成长提示"。
当中国创新药开始在全球舞台崭露头角,我们的临床试验能力也必须完成从"跟跑"到"并跑"的跨越。这不仅需要技术突破,更需要用国际最高标准打磨每一个操作细节。
毕竟,在FDA的眼里,没有"差不多",只有"合规即底线"。
愿下一次,中国CRO交出的核查答卷,写满"NAI"。
完结















0条评论