开篇声明:1:以下内容转自以下内容转自微信公众号 阮博临药微研《FDA临床药理评审报告解读-乌帕替尼(上)》,如有侵权,可联系删除
2. 以下观点,仅代表作者个人观点,请带着质疑的态度去阅读。如有问题,欢迎评论区留言或直接联系作者
阅读FDA的新药临床药理报告,是每一个药物研发人的必修课。今天开始我们定期来跟大家一起解读NDA资料里的临床药理报告。这一期选的药物是乌帕替尼(Upadacitinib),作为艾伯维公司研发的高选择性JAK1抑制剂,已在全球多个市场获批用于治疗类风湿关节炎(RA)及其他免疫性疾病。本文基于FDA的NDA报告中的CLINICAL PHARMACOLOGY AND BIOPHARMACEUTICS REVIEW部分,解读乌帕替尼从Ⅰ期到Ⅲ期的临床试验设计逻辑。
一、总计30项临床研究的整体布局
乌帕替尼的临床开发计划由22项Ⅰ期研究、2项Ⅱ期研究(外加1项在日本开展的Ⅱb/3期支持性研究)和5项Ⅲ期研究构成,同时提交了8项体外研究和3项定量药理学分析报告。
从研究类型分布可以看出,Ⅰ期研究占据了主体地位(22/30),涵盖了PK/BA研究、内在因素影响、外在因素影响、ADME等全方位探索。这种"厚积薄发"的研究策略,确保了后续Ⅱ/Ⅲ期研究的稳健推进。
二、缓释制剂的开发策略:从IR到ER的精准桥接
乌帕替尼的制剂开发经历了一次重要的转型:从速释(IR)胶囊转向缓释(ER)片剂。这一转变并非一蹴而就,而是通过一系列精心设计的相对生物利用度研究逐步推进,最终确立了每日一次的给药方案,并为上市制剂的生物等效性提供了直接证据。
1 核心制剂桥接研究:M14-680的系统性探索
M14-680研究是制剂转换的核心证据之一。该研究设计了六个部分,系统比较了不同制剂和给药方案下的药代动力学(PK)特征。
● Part 1 & 2(单次给药):比较了15 mg/30 mg ER片与12 mg/24 mg IR胶囊的相对生物利用度(BA)。
√ 主要结果: 在空腹条件下,单次给予15 mg和30 mg ER片剂相较于同等总剂量的IR胶囊,AUC(暴露量)相当,但Cmax(峰浓度)降低了约63%。
这表明ER制剂能有效平滑血药浓度峰值。此外,高脂高热饮食使30 mg ER片剂的Cmax和AUC分别增加了20%和17%,提示食物影响较小且无临床意义。
● Part 3(多次给药ER):评估ER片剂多次给药的PK。
√ 主要结果: 每日一次(QD)给药后,稳态在4天内达到,且蓄积极少。15 mg和30 mg QD剂量范围内的PK呈线性比例。
● Part 5 & 6(多次给药桥接):比较15 mg ER QD vs 6 mg IR BID,以及30 mg ER QD vs 12 mg IR BID。
√ 主要结果:多次给药达稳态后,15 mg ER QD与6 mg IR BID的全身暴露量(AUC)相当;30 mg ER QD与12 mg IR BID的全身暴露量(AUC)相当。
这直接证实了ER制剂可以实现每日一次给药,同时维持与有效II期剂量(IR BID)相似的暴露水平,为III期临床选择QD方案奠定了坚实基础。
2 上市前桥接与特殊剂量探索
在确立ER制剂为核心开发方向后,研发团队进一步开展了两项关键的补充研究:
● M15-878研究(上市影像制剂桥接):比较了“上市影像制剂”(To-be-marketed, ER17/ER18)与Ⅲ期临床所用制剂(ER7/ER8)的BA。
√ 主要结果:研究显示,15 mg和30 mg规格的上市制剂与Ⅲ期临床制剂在空腹条件下生物等效(Bioequivalent)(Cmax和AUC的90%置信区间均在80-125%范围内)。
高脂饮食使30 mg上市制剂的Cmax增加40%,AUC增加30%,但这被认为无临床相关性。这一结果确保了商业化批次与临床批次的疗效和安全性一致。
● M16-094研究(高剂量探索):评估了45 mg单一片剂与30 mg+15 mg联合用药的相对BA及食物影响。
√ 主要结果:空腹条件下,单片45 mg ER片剂与15 mg+30 mg两片联用的AUC和Cmax相当。高脂饮食使Cmax和AUC分别增加18%和30%。该研究为未来可能的高剂量适应症拓展储备了关键数据。
3 首次人体研究:M13-401的探索性价值
M13-401作为首次人体试验(FIH),承担了探索剂量范围和建立安全性耐受性基线的重要使命。
√ 主要结果:
剂量递增(SAD):明确了乌帕替尼在健康志愿者中的最大耐受剂量,且Cmax和AUC在1-48 mg范围内呈剂量比例关系。
食物影响:与空腹相比,非空腹条件下给药导致Cmax降低约23%(注:此结果为IR制剂早期数据,后续ER制剂受食物影响表现为轻度增加,但均无临床意义)。
DDI(酮康唑):与强CYP3A4抑制剂酮康唑合用,乌帕替尼的Cmax、AUC0-t和AUCinf分别增加了约70%、76%和75%。这一发现直接导致了说明书中关于“慎与强CYP3A4抑制剂合用”的建议。
4 其他制剂探索:完善证据链的补充研究
● M14-678研究(低剂量ER):比较7.5 mg ER片与2×3 mg IR胶囊的相对BA。
√ 主要结果:7.5 mg ER片相对于3 mg IR BID的相对生物利用度约为66%-86%。该研究为日本等地的低剂量(7.5 mg)适应症开发提供了数据支持。
● M16-552研究(口服溶液):评估口服溶液制剂的BA。
√ 主要结果:空腹条件下,分两次给予6 mg口服溶液(间隔12小时)相较于单次15 mg ER片剂,Cmax高出30%,AUC高出17%。
该数据为儿童用药或吞咽困难患者的未来制剂开发提供了参考,表明溶液剂型可能需要调整剂量以匹配片剂暴露量。
科学意义小结:
通过从首次人体研究(M13-401)到核心制剂桥接(M14-680),再到上市前验证(M15-878)和特殊场景储备(M16-094、M14-678、M16-552)的完整研究链条,乌帕替尼的制剂开发完成了从IR到ER的转型。
关键数据证实15 mg ER QD与6 mg IR BID暴露量相当,30 mg ER QD与12 mg IR BID暴露量相当,且上市制剂与临床制剂生物等效,为NDA申报和后续市场供应奠定了坚实的科学基础。
三、暴露-效应分析:15 mg vs 30 mg的剂量抉择
在剂量选择这一关键决策点上,乌帕替尼的研发团队展现了定量药理学的强大力量,整合了Ⅱ期(M13-537, M13-550)和Ⅲ期研究数据。
1 暴露-疗效关系:平台期的识别
研究团队采用连续时间马尔可夫模型对ACR20/50/70应答率等疗效终点进行建模。
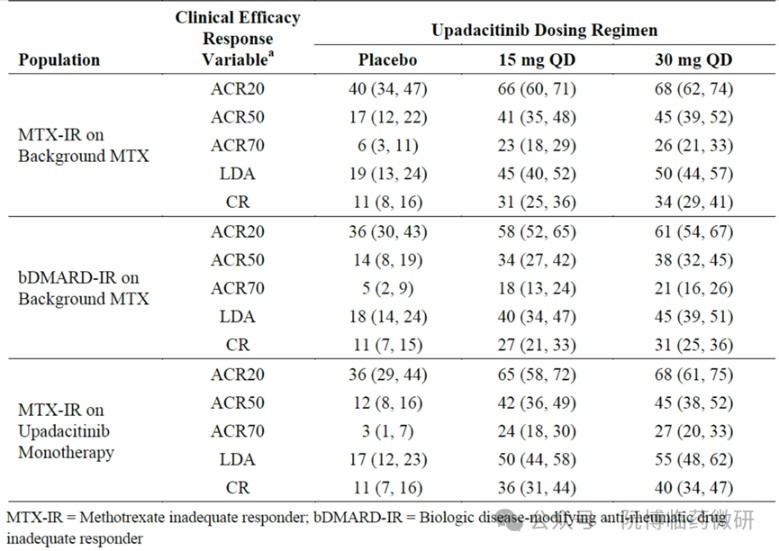
√ 主要结果:模拟结果显示,30 mg QD剂量相较于15 mg QD仅能提供微小的增量疗效获益。例如,在ACR20响应率上,30 mg组虽有数值上的升高趋势,但与15 mg组相比无具有临床意义的显著提升。这表明15 mg QD已达到疗效平台期,更高剂量并不能带来有临床意义的疗效提升。
2 暴露-安全性关系:剂量限制性毒性的识别
安全性分析采用了分层递进的策略,重点考察了血红蛋白、感染等指标。
√ 主要结果:
血红蛋白下降: 血红蛋白下降幅度(>1 g/dL和>2 g/dL)的发生率与药物暴露量呈正相关,30 mg QD组的风险显著高于15 mg QD组。
严重感染: 截至24/26周,严重感染的发生率与暴露量存在关联,高暴露量(对应30 mg剂量)组发生率更高。
其他指标: 肺炎、带状疱疹、血小板变化等未显示明确的暴露-反应关系。
√ 决策结论:
综合疗效与安全性的暴露-效应分析,最终支持选择15 mg QD作为推荐剂量,30 mg QD作为备选方案。
这一决策过程充分体现了"以患者为中心"的药物开发理念——在保证疗效(15 mg已达平台期)的同时,尽可能降低剂量相关的安全风险(如贫血和严重感染)。
总结
通过严谨的暴露-效应分析,乌帕替尼的研发团队在疗效与安全性之间找到了最佳平衡点,最终确立了15 mg这一兼具疗效与安全性的推荐剂量。至此,剂型与剂量两大核心要素已获得充分的临床数据支持。
下一篇,我们将继续解析研发团队如何回答临床应用中不可回避的关键问题:
哪些药物存在合用禁忌?
肝肾功能受损的患者是否需要调整剂量?
以及如何通过群体药代动力学研究整合上千例患者的临床数据,为真实世界的精准用药提供全景式指导。
完结













Kowalevski
还是要关注后续的临床效果
回复dwy
@Kowalevski: 好的
回复