开篇声明:1:以下内容转自以下内容转自微信公众号流行病学与卫生统计学《在日本提交R的考虑》,如有侵权,可联系删除
2. 以下观点,仅代表作者个人观点,请带着质疑的态度去阅读。如有问题,欢迎评论区留言或直接联系作者
ABSTRACT
R的采用和提交是制药编程行业的关键话题,日本也不例外。虽然SAS用户在日本仍然占很大比例,但近年来对R的兴趣显著增长。
日本制药工业协会 (JPMA) 和 PHUSE 等行业组织已经对 R 的采用情况进行了调查,并与日本卫生当局药品和医疗器械管理局 (PMDA) 进行了沟通。PMDA 对接受 R 表现出了开放的态度,赞助商需要考虑 R 提交的最佳方法,包括了解 PMDA 的特定要求 (例如,PMDA 咨询、遵循文档夹结构指南的 PMDA 网关提交等) 。
在本文中,我们将简要介绍PMDA的新药申请(NDA)流程,并重点介绍准备PMDA沟通和R递交的关键点。
INTRODUCTION
截至2025年3月,PMDA已表示愿意接受R作为提交目的。值得注意的是,迄今为止,一家全球制药公司是唯一一家在日本使用R提交的公司。然而,PMDA没有分享有关其经验的实质性信息。
图1显示了日本药品制造商协会(JPMA)在2024年进行的采用R调查的结果。
59%(32/54)的日本制药公司在临床规划活动中使用了 R。32 个回复的详细信息如下:样本量计算(28/32、87.5%)、内部会议分析(23/32、71.9%)、探索性分析(22/32、68.8%)和临床药理学分析(17/32、53.1%)。临床报告活动的用例较少,例如为临床摘要报告创建 SDTM、ADaM 和 TFL。
此外,虽然在临床药理学分析中观察到大多数病例,但制药公司的41%(13/32)和37.5%(12/32)使用了R 和 R程序提交了TLFS。 但是,没有制药公司已将R包提交给PMDA。
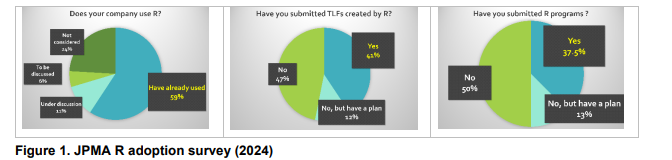
虽然R相关成果已部分提交给PMDA,但日本完整的"R提交"数量仍然非常有限。
SIX POINTS TO CONSIDER FOR PMDA R SUBMISSION
PMDA 的主要关注点是提交 R 代码的执行能力。赞助商必须确保适当的提交前沟通和文档。
PMDA MEETING FOR R SUBMISSION
表1总结了与PMDA R提交相关的PMDA会议。
一种是「NDA前会面」,在NDA前一至三个月举行。NDA前会面的主要目的是让赞助者提前确认他们计划向PMDA提交的文档内容和格式,从而提高提交材料的质量。赞助者也可以通知PMDA他们打算进行基于R的提交。
另一个相关的会议是“关于准备电子研究数据的提交咨询”。在此咨询中,赞助商和PMDA讨论了与R相关可交付成果的电子数据的准备。
我们建议赞助商至少召开一次NDA前会议,通知PMDA他们打算进行基于R的提交。

ADRG DOCUMENTATION
众所周知,PMDA 在 Pinnacle 21 验证器中定义了特定的验证规则。PMDA 和 FDA 在 CDISC 合规性的验证规则上存在差异,这些差异必须在 ADRG 中描述。但是,与 R 相关的描述可以保持一致。
在 ADRG 第 7 节中,申办者必须总结有关 R 的以下分析相关信息:
1. R 和 RStudio 的版本以及分析环境的操作系统版本。
2. 包括版本和描述的 R 软件包信息。
3. 用于 ADaM 和 TLF 的 R 程序。
请注意,必须为 PMDA 指定分析环境的操作系统版本(例如 Windows、Linux、......)。PMDA 强调,这是一个经常被忽视的项目。
FOLDER STRUCTURE (M5)
FDA 和 PMDA 的文档夹结构没有显着差异; 但是,PMDA 不能创建子文档夹。
R 相关信息(程序、软件包) 可以包含在".../analysis/adam/programs"中。

PMDA GATEWAY SYSTEM
当赞助商向 PMDA 提交电子研究数据时,文档通过 PMDA 网关系统提交。
这是一个 PMDA 专用的系统,但与 R 提交没有显着差异。PMDA 网关的文档命名约定与 FDA 电子提交网关几乎相同。文档名必须在 32 个字符以内, 并且仅由字母数字字符(小写)和某些符号(下划线、连字符和单点)组成。
如果单个文档超过 10GB 或一次提交文档的总大小超过 100GB,赞助商应提前通知 PMDA。
R PROGRAMS & R PACKAGES
截至2025年3月,PMDA电子研究数据提交的技术符合指南指出,程序不必可执行。但是,由于对开源软件的接受程度越来越多,将来可能会更新此要求。
如果提交R软件包具有挑战性,则赞助商可以提交一个规范文档,其中包含包装版本信息和所使用软件包的详细信息,而不是提交R代码和软件包(PMDA技术符合指南,第4.1.6.1节)。
此外,R联盟Pilot 3项目提供了提交R代码和R软件包的一个很好的例子。赞助商可能遵循相同的方法。可以在PMDA咨询中进行进一步的讨论。
R PACKAGE MANAGEMENT
R 包管理不是 PMDA R 提交的特定考虑因素,R 包的验证是赞助商的责任。
冻结分析环境,包括 R 包管理,对于在提交后响应inquiries进行分析至关重要。
对于 PMDA 检查,建议赞助商准备一份 R 包管理文档,包括系统验证报告,以及 ADaM 和 TFL QC 报告。
THE RECOMMENDED PROCESS TOWARD PMDA R SUBMISSION
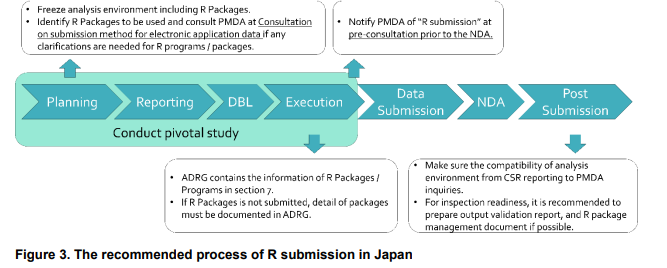
图3显示了PMDA R提交的建议流程。
第一步是列出要使用的R软件包。如果赞助商计划提交内部开发的R软件包,则应始终考虑与PMDA协商。一般来说,建议使用CRAN的公共可用R软件包以避免不必要的讨论,因为验证内部开发的软件包可能非常耗时。
其次,分析数据审查员指南 (ADRG) 应包括有关 R 分析环境、代码和软件包的关键信息。如果提交 R 代码和软件包有困难,应在 ADRG 第 7 节中提供分析算法的详细信息。
最后,申办者应告知 PMDA R 提交情况,以便 PMDA 能够确认。申办者还应为 PMDA 和检查部门可能提出的问题做好准备,以确保结果的可重复性。
如果eStudy数据包含与R提交相关的新类型数据,则应考虑就提交方法进行磋商。例如,这适用于分析元数据,例如与CDISC分析结果标准相关的LinkML。赞助商可以与PMDA讨论提交此类新类型的数据。
CONCLUSION
虽然FDA和PMDA之间在eStudy数据提交方面存在一些差异,但R提交的要求预计大致相同。然而,强烈建议计划PMDA咨询,特别是首次在公司R提交中提交R包时。关于向PMDA提交R仍有许多不确定性。但是,如果领先的公司主动分享信息,它将增强行业内的整体理解,并最终有助于更快地批准新药。
REFERENCES
PMDA, “Revision of Technical Conformance Guide on Electronic Study Data Submissions”, April 8, 2024.
PMDA, “New Drug Applications Using the Gateway System”, April 1, 2022.
JPMA, 2024, “OSS surveillance in Japan” (Japanese only) Accessed March 20, 2025.
https://www.jpma.or.jp/information/evaluation/results/allotment/eo4se30000002zrxatt/DS_202412_oss_questionaire.pdf
R Submission Working Group, Available at https://rconsortium.github.io/submissions-wg/
Yuichi Nakajima, PHUSE EU Connect 2021, “(You) R Programs for Health Authorities in Japan”
完结
原文链接:https://mp.weixin.qq.com/s/toMiWhGfTd5KegaAPRvcew














Almeida
原来如此!😯
回复