開篇宣告:1:以下內容轉自以下內容轉自微信公眾號流行病學與衛生統計學《在日本提交R的考慮》,如有侵權,可聯絡刪除
2. 以下觀點,僅代表作者個人觀點,請帶著質疑的態度去閱讀。如有問題,歡迎評論區留言或直接聯絡作者
ABSTRACT
R的採用和提交是製藥程式設計行業的關鍵話題,日本也不例外。雖然SAS使用者在日本仍然佔很大比例,但近年來對R的興趣顯著增長。
日本製藥工業協會 (JPMA) 和 PHUSE 等行業組織已經對 R 的採用情況進行了調查,並與日本衛生當局藥品和醫療器械管理局 (PMDA) 進行了溝通。PMDA 對接受 R 表現出了開放的態度,贊助商需要考慮 R 提交的最佳方法,包括瞭解 PMDA 的特定要求 (例如,PMDA 諮詢、遵循文件夾結構指南的 PMDA 閘道器提交等) 。
在本文中,我們將簡要介紹PMDA的新藥申請(NDA)流程,並重點介紹準備PMDA溝通和R遞交的關鍵點。
INTRODUCTION
截至2025年3月,PMDA已表示願意接受R作為提交目的。值得注意的是,迄今為止,一家全球製藥公司是唯一一家在日本使用R提交的公司。然而,PMDA沒有分享有關其經驗的實質性資訊。
圖1顯示了日本藥品製造商協會(JPMA)在2024年進行的採用R調查的結果。
59%(32/54)的日本製藥公司在臨床規劃活動中使用了 R。32 個回覆的詳細資訊如下:樣本量計算(28/32、87.5%)、內部會議分析(23/32、71.9%)、探索性分析(22/32、68.8%)和臨床藥理學分析(17/32、53.1%)。臨床報告活動的用例較少,例如為臨床摘要報告建立 SDTM、ADaM 和 TFL。
此外,雖然在臨床藥理學分析中觀察到大多數病例,但製藥公司的41%(13/32)和37.5%(12/32)使用了R 和 R程式提交了TLFS。 但是,沒有製藥公司已將R包提交給PMDA。
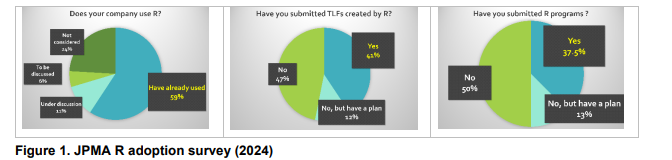
雖然R相關成果已部分提交給PMDA,但日本完整的"R提交"數量仍然非常有限。
SIX POINTS TO CONSIDER FOR PMDA R SUBMISSION
PMDA 的主要關注點是提交 R 程式碼的執行能力。贊助商必須確保適當的提交前溝通和文件。
PMDA MEETING FOR R SUBMISSION
表1總結了與PMDA R提交相關的PMDA會議。
一種是「NDA前會面」,在NDA前一至三個月舉行。NDA前會面的主要目的是讓贊助者提前確認他們計劃向PMDA提交的文件內容和格式,從而提高提交材料的質量。贊助者也可以通知PMDA他們打算進行基於R的提交。
另一個相關的會議是“關於準備電子研究資料的提交諮詢”。在此諮詢中,贊助商和PMDA討論了與R相關可交付成果的電子資料的準備。
我們建議贊助商至少召開一次NDA前會議,通知PMDA他們打算進行基於R的提交。

ADRG DOCUMENTATION
衆所周知,PMDA 在 Pinnacle 21 驗證器中定義了特定的驗證規則。PMDA 和 FDA 在 CDISC 合規性的驗證規則上存在差異,這些差異必須在 ADRG 中描述。但是,與 R 相關的描述可以保持一致。
在 ADRG 第 7 節中,申辦者必須總結有關 R 的以下分析相關資訊:
1. R 和 RStudio 的版本以及分析環境的作業系統版本。
2. 包括版本和描述的 R 軟體包資訊。
3. 用於 ADaM 和 TLF 的 R 程式。
請注意,必須為 PMDA 指定分析環境的作業系統版本(例如 Windows、Linux、......)。PMDA 強調,這是一個經常被忽視的專案。
FOLDER STRUCTURE (M5)
FDA 和 PMDA 的文件夾結構沒有顯著差異; 但是,PMDA 不能建立子文件夾。
R 相關資訊(程式、軟體包) 可以包含在".../analysis/adam/programs"中。

PMDA GATEWAY SYSTEM
當贊助商向 PMDA 提交電子研究資料時,文件透過 PMDA 閘道器系統提交。
這是一個 PMDA 專用的系統,但與 R 提交沒有顯著差異。PMDA 閘道器的文件命名約定與 FDA 電子提交閘道器幾乎相同。文件名必須在 32 個字元以內, 並且僅由字母數字字元(小寫)和某些符號(下劃線、連字元和單點)組成。
如果單個文件超過 10GB 或一次提交文件的總大小超過 100GB,贊助商應提前通知 PMDA。
R PROGRAMS & R PACKAGES
截至2025年3月,PMDA電子研究資料提交的技術符合指南指出,程式不必可執行。但是,由於對開源軟體的接受程度越來越多,將來可能會更新此要求。
如果提交R軟體包具有挑戰性,則贊助商可以提交一個規範文件,其中包含包裝版本資訊和所使用軟體包的詳細資訊,而不是提交R程式碼和軟體包(PMDA技術符合指南,第4.1.6.1節)。
此外,R聯盟Pilot 3專案提供了提交R程式碼和R軟體包的一個很好的例子。贊助商可能遵循相同的方法。可以在PMDA諮詢中進行進一步的討論。
R PACKAGE MANAGEMENT
R 包管理不是 PMDA R 提交的特定考慮因素,R 包的驗證是贊助商的責任。
凍結分析環境,包括 R 包管理,對於在提交後響應inquiries進行分析至關重要。
對於 PMDA 檢查,建議贊助商準備一份 R 包管理文件,包括系統驗證報告,以及 ADaM 和 TFL QC 報告。
THE RECOMMENDED PROCESS TOWARD PMDA R SUBMISSION
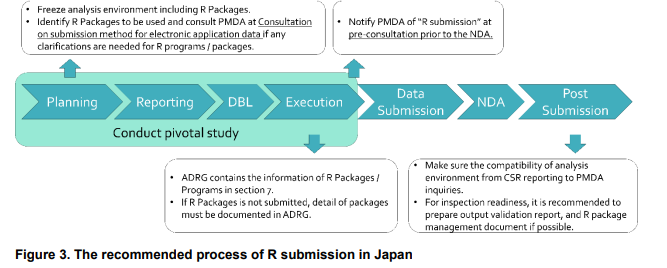
圖3顯示了PMDA R提交的建議流程。
第一步是列出要使用的R軟體包。如果贊助商計劃提交內部開發的R軟體包,則應始終考慮與PMDA協商。一般來說,建議使用CRAN的公共可用R軟體包以避免不必要的討論,因為驗證內部開發的軟體包可能非常耗時。
其次,分析資料審查員指南 (ADRG) 應包括有關 R 分析環境、程式碼和軟體包的關鍵資訊。如果提交 R 程式碼和軟體包有困難,應在 ADRG 第 7 節中提供分析演算法的詳細資訊。
最後,申辦者應告知 PMDA R 提交情況,以便 PMDA 能夠確認。申辦者還應為 PMDA 和檢查部門可能提出的問題做好準備,以確保結果的可重複性。
如果eStudy資料包含與R提交相關的新型別資料,則應考慮就提交方法進行磋商。例如,這適用於分析後設資料,例如與CDISC分析結果標準相關的LinkML。贊助商可以與PMDA討論提交此類新型別的資料。
CONCLUSION
雖然FDA和PMDA之間在eStudy資料提交方面存在一些差異,但R提交的要求預計大致相同。然而,強烈建議計劃PMDA諮詢,特別是首次在公司R提交中提交R包時。關於向PMDA提交R仍有許多不確定性。但是,如果領先的公司主動分享資訊,它將增強行業內的整體理解,並最終有助於更快地批准新藥。
REFERENCES
PMDA, “Revision of Technical Conformance Guide on Electronic Study Data Submissions”, April 8, 2024.
PMDA, “New Drug Applications Using the Gateway System”, April 1, 2022.
JPMA, 2024, “OSS surveillance in Japan” (Japanese only) Accessed March 20, 2025.
https://www.jpma.or.jp/information/evaluation/results/allotment/eo4se30000002zrxatt/DS_202412_oss_questionaire.pdf
R Submission Working Group, Available at https://rconsortium.github.io/submissions-wg/
Yuichi Nakajima, PHUSE EU Connect 2021, “(You) R Programs for Health Authorities in Japan”
完結
原文連結:https://mp.weixin.qq.com/s/toMiWhGfTd5KegaAPRvcew













Almeida
原來如此!😯
回覆